


БНБ
"БРОКГАУЗ И ЕФРОН" (121188)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Хлороолефины
Определение "Хлороолефины" в словаре Брокгауза и Ефрона
Хлороолефины (хим.) — X. отвечают по составу углеводородам этиленного ряда (олефинам) C nH2n, в которых один или несколько атомов водорода замещены хлором. Названия этих соединений, обыкновенно, производятся от названий углеводородов с приставкой "хлоро"; расположение атомов Cl в углеводородной цепи обозначается греческими буквами, считая от места двойной связи; различают также симметрические и несимметрические формы, напр.: СН 2:СН.СН 2Cl — γ-хлоропропилен (хлористый аллил) и СНCl:СНCl — симметрический дихлороэтилен. Общий способ получения X. состоит в отнятии элементов хлористого водорода от дву- и более замещенных хлоропарафинов (см.) действием алкогольного едкого кали или алкоголятов, напр.:
СН 2 Cl.СН 2Cl + KOH = CH2Cl:CH2 + KCl + H2O;
СН 3 СНC l2 + NaO.C2H5 = СН 2:СНCl NaCl + С 2H5 ОН;
СН 2 Cl.СНCl 2 + КОН = CHCl:CHCl + KCl + H 2O.
Элементы хлористого водорода выделяются всегда от соседних атомов углерода; поэтому, когда такое выделение может совершиться двояко, одновременно образуются оба возм. изомера, напр.:
СН 3.СНCl.СН 2 Cl + КОН = СН 2:СНСН 2 Cl + КCl + Н 2 О:СН 3.СНCl. CН 2 Cl + КOН = CH 3.CCl:CH2 + КCl + Н 2 О.
При прямом действии хлора на олефины X. образуются лишь в исключительных случаях, как продукты разложения образовавшегося первоначально хлоропарафина. Возможно, наконец, получать X., присоединяя 1 частицу хлористо-водородной кислоты или хлора к ацетиленовым углеводородам, напр.:
CН:СН + НCl = СН 2:СНCl;
СН 3.СН:СН + Cl = CH 3.CHCl:СHCl.
За исключением газообразного хлороэтилена X. представляют собою бесцветные жидкости, физические свойства которых изменяются в такой же зависимости от степени замещения и от изомерии, как и в предельном ряду (см. Хлоропарафины). Химические свойства этих соединений, обусловленные нахождением в них двойной связи, сказываются в способности к реакциям присоединения галоидов и галоидоводородных кислот. Последние присоединяются к X. менее энергично, чем к самим олефинам, и реакции эти протекают не так правильно, как там. Подобно хлоропарафинам, X. могут обменивать галоид на различные другие остатки, напр., на гидроксил:
СН 2:СН.СН 2 Сl + Н 2 О = СН 2:СН.СН 2.ОН.
В этом отношении хлор, стоящий при атоме углерода, связанном двойной связью (группы:СHCl и:CCl), отличается своей неспособностью обмениваться на гидроксил: вместо непредельных спиртов при гидратации таких соединений получаются альдегиды и кетоны, напр.:
СН 2:СНCl + H 2O = CH3.CHO + HCl;
СН 3.СCl:СН 2 + Н 2 О = (СН 3)2 СО + НCl.
Интересной особенностью несимметрических X. является их способность полимеризоваться, переходя в аморфные, нерастворимые модификации, чем они существенно отличаются от симметрических изомеров. Монохлороэтилен, СН 2:CНCl, темп. кип. — 18°; дихлороэтилен несимм., CH 2:CCl2, темп. кип. 37°; симм., CHCl:CHC 2, темп. кип. 55°; трихлороэтилен, СНCl:СCl 2, темп. кип. 88°; перхлороэтилен, CCl:CCl2, темп. кип. 121°; α-хлоропропилен CH3.CH:CHCl, темп. кип. 35°; β-хлоропропилен, СН 3.ССl:СН 2, темп. кип. 23°; γ-хлоропропилен. СH 2 Cl.СH:СH 2 (хлористый аллил), темп. кип. 46°. Кроме приведенных трех возможных по теории строения монохлоропропиленов стереохимическая гипотеза предвидит еще существование стереоизомерных α-продуктов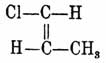
и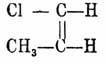
которые описаны Вислиценусом, но до сих пор еще прочно не установлены.
Д. Монастырский. Δ.
| "БРОКГАУЗ И ЕФРОН" >> "Х" >> "ХЛ" >> "ХЛО" >> "ХЛОР" |
Статья про "Хлороолефины" в словаре Брокгауза и Ефрона была прочитана 594 раз
| Коптим скумбрию в коробке |
| Кимчи из грибов |
TOP 15
- Волос
- Проно
- Степные животные
- Гимнастика
- Индийский океан
- Архитектура
- Сравнение, в литературе
- Манда
- Клитры
- Колесование
- Испарение
- Травоядные животные
- Оплодотворение у pacтений
- Вредные насекомые
- Электризация тел