


БНБ
"БРОКГАУЗ И ЕФРОН" (121188)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Фенилмолочные кислоты
Определение "Фенилмолочные кислоты" в словаре Брокгауза и Ефрона
Фенилмолочные кислоты или фенилоксипропионовые С 6 Н 5 —С 2 Н 3 (ОН)—СO 2 —Н. — Теоретически возможно представить 4 структурно изомерных Ф. кисл. приведенной формулы, и все эти изомеры известны в действительности: 1) β-фенилгидракриловая кисл. С 6 Н 5 —СН(ОН)—С 2 —СO 2 Н; 2) α - фенилгидракриловая кисл. СН 2 (ОН)—СН—(С 6 Н 5)—СO 2 Н; 3) β-Ф. кисл. С 6 Н 5 —СН 2 —СН(ОН)—СO 2 Н; 4) α-Ф. кислота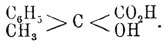
Приведенные формулы Ф. кислот указывают, что каждый из изомеров имеет в своем составе один асимметрический атом углерода (см. Стереоизомерия) и потому можно ожидать для каждой из Ф. кислот трех модификаций, из которых одна должна вращать поляризованный свет вправо, другая влево и третья — эквимолекулярная смесь первых двух — должна быть инактивна. До сих пор, однако, эти три стереоизомерных модификации известны только для α -фенилгидракриловой, или троповой, кислоты.
β - Фенилгидракриловая, или обыкновенная Ф. кислота. Легко получается при кипячении 1 ч. β-бромгидрокоричной кислоты с 10 ч. воды или при восстановлении амальгамой натрия α-хлор-β-фенилгидракриловой кислоты, получающейся присоединением хлорноватистой кислоты НСlО к коричной. Ф. кислота кристаллизуется в бесцветных призмах, плавящихся при 93°. Она очень хорошо растворима в холодной воде, а с горячей водой смешивается во всех пропорциях. Нагретая до 180° или при кипячении с баритовой водой, она распадается на коричную кислоту и воду:
С 6 Н 5 —СН(OH)—CH 2—CO2 H = С 6 Н 5 —СН=CH—CO 2 Н + Н 2O.
При кипячении с разбавленной серной кислотой этот распад совершается быстро, но при этом образуются еще небольшие количества стирола С 6 Н 5 СН=СН 2. При смешении с сильно концентрированными HBr или HJ-кислотами Ф. кислота переходит в соответствующие β-галоидогидрокоричные кислоты.
а-Фенилгидракриловая, или троповая кисл., как было указано выше, известна в трех модификациях: инактивная троповая кислота плавится при 117° и получается нагреванием при 60° алкалоидов атропина и гиосциамина с баритовой водой:
C17H23NO3 (атропин) + Н 2O = C8H15 NO (тропин) + СН 2 (ОН)—СН(С 6 Н 5)—СO 2 Н.
Синтетически троповая кислота приготовлена, исходя из α-Ф. кисл.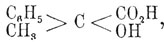
которая при нагревании с НСl (см. ниже) легко теряет воду и переходит в атроповую кислоту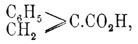
которая с концентрированной соляной кислотой дает β-хлоргидратроповую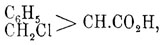
a эта последняя при обмыливании раствором поташа превращается в троповую. Троповая кисл., подобно обыкновенной Ф. кисл., легко растворима в холодной воде и смешивается во всех пропорциях с горячей водой. При нагревании с Н 2 O до 130° она не изменяется. Потеря молекулы воды совершается ею только при продолжительном кипячении ее с баритовой водой, причем образуется атроповая кислота С 9 Н 8O2, при нагревании же с концентрированной соляной кислотой до 140° хотя и происходит та же потеря элементов Н 2 O, но здесь образуется изоатроповая кислота (С 9 Н 8O2)2.
β -Ф. кислота кристаллизуется из воды в больших призмах, плавящихся при 97—98°. При 130° распадается, в противоположность остальным Ф. кислотам, не на воду и новую кислоту, а на муравьиную кислоту HCO 2 H и α-толуиловый альдегид
С 6 Н 5 СН 2 —СНО=С 6 Н 5 —СН 2 —СН(ОН)—СO 2 Н = С 6 Н 5 СН 2 —СНО + Н 2 СО 2.
α -Ф., или атролактиновая кислота. Получается обмыливанием раствором соды α-бромгидротроповой кислоты. Кристаллизуется из воды в иглах или ромбических пластинках состава С 9 Н 10O3 + 1/2H2 O, плавящихся при 90—91°; при нагревании до 80—85° кристаллы теряют воду, и тогда безводная кислота плавится уже при 93—94°. При кипячении с баритовой водой α-Ф. кислота почти не разлагается; но при кипячении с крепкой соляной кислотой она теряет воду и переходит в атроповую кислоту.
Д. X.
| "БРОКГАУЗ И ЕФРОН" >> "Ф" >> "ФЕ" >> "ФЕН" |
Статья про "Фенилмолочные кислоты" в словаре Брокгауза и Ефрона была прочитана 1241 раз
| Салат тофу |
| Салат тофу |
TOP 15
- Волос
- Проно
- Степные животные
- Гимнастика
- Индийский океан
- Архитектура
- Сравнение, в литературе
- Манда
- Клитры
- Колесование
- Испарение
- Травоядные животные
- Оплодотворение у pacтений
- Вредные насекомые
- Электризация тел