


БНБ
"БРОКГАУЗ И ЕФРОН" (121188)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Салициловая кислота
Определение "Салициловая кислота" в словаре Брокгауза и Ефрона
Салициловая кислота (хим.) С 7 Н 6 О 3 = С 6 Н 4 (ОН)—СО 2 Н — является представительницей ароматических оксикислот. С. кислота в виде соединений со спиртами (эфиров) часто встречается в растительном царстве; так, ее эфиры находятся в цветах Spirеа ulmaria, в эфирном масле Gaulteria procumbens и некотор. вересковых (Ericaceae). Открыта она была Пириа 1838 г. Этот химик, исследуя продукты распада салицина, глюкозида, находящегося в корнях и листьях Salix helix, выделил салициловый альдегид C 6H4 (OH)CHO, который при сплавлении с едким кали, подобно всем альдегидам, распался на кислоту, которую он и назвал салициловой, и соответствующий спирт — салигенин (см.). Через год после этого открытия Лёвиг и Видеман открыли С. кислоту в цветах Spirca ulmaria, а в 1843 г. Кагур показал, что главная составная часть гаултерового масла есть С.-этиловый эфир С 6 Н 4 (ОН)—СО 2 С 2 Н 5. Исследования этих ученых касались гл. образом констатирования присутствия С. кисл. в тех или других продуктах растительного царства, и они совершенно не касались строения С. кислоты, которую просто принимали за двухосновную кислоту, и только благодаря трудам Gerhardt'a (1853 г.) и Кольбе (1860 г.) возможно было установить рациональную формулу С. кислоты, которая теперь рассматривается как ортооксибензойная кислота, Кольбе же первый и синтезировал С. кисл., открыв при этом довольно общий способ получения ортооксикислот ароматического ряда. Этот ученый показал, что феноляты натрия способны фиксировать при высокой темп. угольный ангидрид и превращаться при этом в натровые соли ортооксикислот:
2C6H5ONa + CO2 = C6H4(ONa)CO2Na+C6H5(OH).
Замечательно, что эта реакция идет только с фенолятами натрия, другие же металлы дают в этом случае соли метаоксикислот. Теперь этот способ получения С. кислоты приобрел громадное значение в технике, и вся С. кислота готовится по нему, и только сравнительно очень недавно в технику начал проникать способ получения С. — Р. Шмитта, который показал, что при большом давлении фенолят натрия соединяется с угольным ангидридом на холоде, давая фенолоуглекислый натр C 6H5O—CO2 Na, т. е. натровую соль кислого фенилугольного эфира 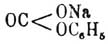 , которая в свою очередь под давлением и при 120—130° нацело превращается в салицилово-натриевую соль. Салициловая кислота кристаллизуется бесцветными иголками сладковато-кислого вкуса. Она довольно трудно растворима в холодной воде и легко в горячей и спирте. Ее водные растворы с хлорным железом дают характерное, очень интенсивное фиолетовое окрашивание. Как оксикислота, она способна со спиртами давать два ряда эфиров, кислые и средние, напр. C 6H4(OH)CO3CH2 и С 6 Н 4 (ОСН 3)СО 2 СН 3. Кроме того, средние эфиры при неполном обмыливании едким кали дают эфирокислоты, напр. С 6 Н 4 (ОСН 3)—СО 2 СН 2 + KHO = С 6 Н 4 (ОСН 3)СО 2 К + СН 3 ОН. Из вышеприведенных производных имеют значение главным образом кислые эфиры, легко получаемые кипячением С. кислоты с соответствующим спиртом в присутствии серной кислоты или при пропускании через кипящую смесь С. кислоты со спиртом сухого хлористоводородного газа. Кислый метильный эфир С 6 Н 4 (ОH)CО 2CH3 известен в продаже под названием гаултерового масла (Wintergr ü nol); это — жидкость удельн. веса 1,197, кипящая при 224°, обладает приятным запахом, несколько напоминающим гиацинты. При нагревании С. кислоты с фенолом и хлорокисью фосфора РОСl 3 образуется кислый фенильный эфир С 6 Н 4 (ОН)CО 2 —С 6 Н 5, известный под названием салола (см.). Если вместо фенола взять тиофенол, то получается тиосалол С 6 Н 4(OH)CO—S—C6H5 — хорошее антисептическое средство. При нагревании одной С. кислоты или в присутствии водоотнимающих средств образуются разнообразные продукты уплотнения ее и между прочим ксантон
, которая в свою очередь под давлением и при 120—130° нацело превращается в салицилово-натриевую соль. Салициловая кислота кристаллизуется бесцветными иголками сладковато-кислого вкуса. Она довольно трудно растворима в холодной воде и легко в горячей и спирте. Ее водные растворы с хлорным железом дают характерное, очень интенсивное фиолетовое окрашивание. Как оксикислота, она способна со спиртами давать два ряда эфиров, кислые и средние, напр. C 6H4(OH)CO3CH2 и С 6 Н 4 (ОСН 3)СО 2 СН 3. Кроме того, средние эфиры при неполном обмыливании едким кали дают эфирокислоты, напр. С 6 Н 4 (ОСН 3)—СО 2 СН 2 + KHO = С 6 Н 4 (ОСН 3)СО 2 К + СН 3 ОН. Из вышеприведенных производных имеют значение главным образом кислые эфиры, легко получаемые кипячением С. кислоты с соответствующим спиртом в присутствии серной кислоты или при пропускании через кипящую смесь С. кислоты со спиртом сухого хлористоводородного газа. Кислый метильный эфир С 6 Н 4 (ОH)CО 2CH3 известен в продаже под названием гаултерового масла (Wintergr ü nol); это — жидкость удельн. веса 1,197, кипящая при 224°, обладает приятным запахом, несколько напоминающим гиацинты. При нагревании С. кислоты с фенолом и хлорокисью фосфора РОСl 3 образуется кислый фенильный эфир С 6 Н 4 (ОН)CО 2 —С 6 Н 5, известный под названием салола (см.). Если вместо фенола взять тиофенол, то получается тиосалол С 6 Н 4(OH)CO—S—C6H5 — хорошее антисептическое средство. При нагревании одной С. кислоты или в присутствии водоотнимающих средств образуются разнообразные продукты уплотнения ее и между прочим ксантон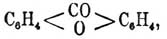
хромогенное вещество многих желтых красок.
Д. А. Хардин. Δ.
С. кислота — врачебное применение. Белый, объемистый порошок или мельчайшие, блестящие, игольчатые кристаллы, без запаха, сладковато-кислого, раздражающего вкуса, растворяется в 500 чч. холодной и в 15 чч. горячей воды, в 2,5 ч. спирта, 2 ч. эфира, 80 ч. хлороформа, 60 ч. глицерина, 70 ч. жирного масла; плавится при 157°. С. кислота одно время добывалась из коры некоторых видов ивы (Salix — откуда и название этой кислоты).
Салицилокислый натрий — белый кристаллический порошок, растворяется в 0,9 част. воды, в 6 ч. алкоголя, содержит 14,38% натрия и 85,62% частей С. кислоты. С. кислота и ее натриевая соль нашли широкое применение во врачебной практике начиная с конца 70 годов, когда обращено было внимание на весьма успешное лечение этими препаратами острого суставного ревматизма. Благоприятные результаты при таком заболевании, против которого не было до того времени сколько-нибудь надежных средств, послужили толчком к введению в терапию целой серии новых препаратов, нашедших широкое практическое применение и немало способствовавших разъяснению некоторых весьма важных вопросов патологии, терапии и фармакологии. Так как острый суставный ревматизм вызывается болезнетворным микроорганизмом (хотя точно до сих пор не определенным) и характеризуется главным образом повышением температуры тела и ощущением боли в суставах, то С. кислота, устраняя такое заболевание, должна, следовательно, действовать на самую причину болезни или же, кроме того, на явления, сопутствующие заболеванию, а именно парализовать болевую чувствительность и понизить повышенную температуру. Ввиду этого фармакологическое исследование имеет целью изучение антисептических, жаропонижающих и болеутоляющих свойств С. кислоты и вместе с тем ознакомление с другими сторонами действия этих препаратов.
Противобродильные и противогнилостные свойства. Минимальные количества С. кислоты останавливают брожение виноградного сахара, парализуя деятельность дрожжевого грибка. Раствор 1:1000 задерживает развитие плесени; раствор 1:3000 задерживает рост сибиреязвенных палочек; 1 часть С. кислоты на 1500 воды вызывает полную остановку в развитии бацилл сибирской язвы. В 0,4% растворе предотвращается гнилостное разложение мяса. Несмотря, однако, на столь значительные антисептические свойства, С. кислота как обеззараживающее вещество имеет в медицине сравнительно малое применение, отчасти вследствие трудной растворимости, главным же образом, вследствие того, что она легко вступает в соединение с фосфорнокислыми и углекислыми солями, значительно теряя при этом свои дезинфицирующие свойства.
Влияние на температуру. С. кислота и ее натронная соль в терапевтических дозах не вызывает у здоровых людей понижения t° тела, у лихорадящих же, в зависимости от формы заболевания — значительно понижает повышенную температуру. Понижение особенно резко выступает при остром суставном ревматизме. Падение температуры под влиянием этих средств зависит от увеличенной теплоотдачи благодаря расширению сосудов и обильному потоотделению, но возможно, что такое действие отчасти обусловливается также уменьшением окислительных процессов в теле. Значительное понижение t° при остром суставном ревматизме не может быть объяснено исключительно процессами образования и потери тепла, так как такого понижения не наблюдается в других лихорадочных формах. Очевидно, что при остром ревматизме С. кислота устраняет самую причину, вызвавшую чрезмерное нагревание тела. Опыты на животных показывают, что С. кислота и ее натронная соль в умеренных дозах оказывают весьма слабое влияние на центральную нервную систему, равно также на периферические окончания чувствительных нервных волокон. Явления угнетения нервной системы наблюдаются только после применения токсических доз. Наблюдения над здоровыми людьми подтверждают экспериментальные исследования над животными. Но при остром суставном ревматизме С. кислота весьма резко уменьшает болезненность в суставах настолько, что больной, вынужденный соблюдать самый строгий покой из-за боязни сильной болезненности, после приема С. кислоты может без посторонней помощи принять то или другое положение в постели. Применение С. кислоты послужило толчком к введению во врачебную практику весьма важных жаропонижающих и болеутоляющих средств, благодаря которым современная терапия может во многих случаях обойтись без назначения различных отвлекающих средств, каковы банки, пиявки, горчичники, мушки, нарывные мази и др. С. кислота при внутреннем употреблении вызывает довольно сильное раздражение слизистых оболочек пищеварительного канала, поэтому ее обыкновенно заменяют более растворимой и менее раздражающей натронной солью. Ее назначают по 0,25 — 0,50 — 1,0 несколько раз в день в порошках или в растворе при суставном ревматизме, при серозном плеврите, против инфлуэнцы и гриппа, иногда при подагре и желчной колике. С. кислота применяется почти исключительно снаружи, в смеси с каким-нибудь жиром или вазелином (1 ч. на 10 ч. жира), в виде мазей, напр. при мокнущей экземе; в смеси с 90% крахмала и 5% талька — как присыпка против потливости ног; для пропитывания перевязочных материалов (3—10% вата, марли или юта); в растворах (1:1000) для промываний ран, гнойных полостей. С. кислота и С. натрий, всасываясь со слизистых оболочек и поверхностей ран, нередко вызывали тяжелые побочные явления, всего чаще со стороны почек, через которые выводится большая часть введенных в организм С. препаратов. Поэтому при воспалительных явлениях в почках средства эти назначаются только в крайних случаях. При слабой деятельности сердца также необходимо быть осторожным, в особенности с назначением больших доз. Воспалительные явления среднего уха могут служить противопоказанием к назначению С. препаратов, так как последние, вызывая расширение сосудов, могут обусловить появление кровоизлияния в барабанной полости.
Д. Каменский.
| "БРОКГАУЗ И ЕФРОН" >> "С" >> "СА" >> "САЛ" >> "САЛИ" |
Статья про "Салициловая кислота" в словаре Брокгауза и Ефрона была прочитана 2165 раз
| Коптим скумбрию в коробке |
| Вкуснейшие куриные леденцы |
TOP 15
- Волос
- Проно
- Степные животные
- Гимнастика
- Индийский океан
- Архитектура
- Сравнение, в литературе
- Манда
- Клитры
- Колесование
- Испарение
- Травоядные животные
- Оплодотворение у pacтений
- Вредные насекомые
- Электризация тел