


БНБ
"БРОКГАУЗ И ЕФРОН" (121188)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Гремучая кислота
Определение "Гремучая кислота" в словаре Брокгауза и Ефрона
Гремучая кислота — Г. кислота, отвечающая гремучим солям (см.), в свободном виде не получена. О строении и причинах непрочности Г. кислоты судят по свойствам и превращениям гремучих солей (фульминатов). Вопрос о строении Г. кисл. важен для установления более выгодных и удобных способов получения фульминатов, нежели существующие. Работы Нефа и Шолля дают возможность приписать Г. кислоте строение 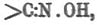 в противоположность формуле Штейнера
в противоположность формуле Штейнера  . Последняя основана главным образом на синтетических реакциях получения фульминатов; кроме обычного синтеза гремучей ртути, окислением этилового спирта азотной кислотой в присутствии Hg(NO 3)2, Штальшмидт (1894) получил ее окислением лигнона (см. соотв. статью) в тех же условиях. Л. Вёлер и Теодорович (1905) получили гремучую ртуть из диметилацеталя, диэтилацеталя, ацетальдегида, паральдегида и метальдегида, тогда как ни метиловый (как это давно было известно), ни пропиловые, ни аллиловые спирты, так же как и альдегиды: формальдегид, пропиловый, изобутиловый и кетоны: ацетон, метилэтилкетон, не дают фульминатов при окислении азотной кислотой в присутствии Hg(NO 3)2 [По опытам Велера и Теодоровича, эта реакция вообще идет только с NHO 3, содержащей окислы азота]. Авторы говорят поэтому, что гремучие соли могут получаться окислением тел, содержащих метильную группу в связи с группировками:
. Последняя основана главным образом на синтетических реакциях получения фульминатов; кроме обычного синтеза гремучей ртути, окислением этилового спирта азотной кислотой в присутствии Hg(NO 3)2, Штальшмидт (1894) получил ее окислением лигнона (см. соотв. статью) в тех же условиях. Л. Вёлер и Теодорович (1905) получили гремучую ртуть из диметилацеталя, диэтилацеталя, ацетальдегида, паральдегида и метальдегида, тогда как ни метиловый (как это давно было известно), ни пропиловые, ни аллиловые спирты, так же как и альдегиды: формальдегид, пропиловый, изобутиловый и кетоны: ацетон, метилэтилкетон, не дают фульминатов при окислении азотной кислотой в присутствии Hg(NO 3)2 [По опытам Велера и Теодоровича, эта реакция вообще идет только с NHO 3, содержащей окислы азота]. Авторы говорят поэтому, что гремучие соли могут получаться окислением тел, содержащих метильную группу в связи с группировками: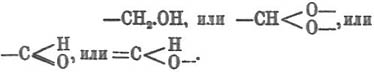
Формула Нефа-Шолля изображает Г. кислоту как оксим окиси углерода; углерод признается в Г. кислоте двухатомным. За эту формулу говорят след. факты: 1) нет кислых гремучекислых солей [Типичные двуосновные кислоты: дитионовая, H 2S2O6 и гидросернистая, Н 2S2O4, также, впрочем, не дают кислых солей.]; 2) при разложении гремучей ртути соляной кислотой получается муравьиная, а не щавелевая кислота; 3) гремучее серебро и гремученатровая соль дают при действии НСl (при 0°) продукт присоединения частицы НСl к Г. кислоте, хлористый формилоксим, который может быть переведен обратно с количественным выходом — в гремучие соли (Неф и Шолль); 4) образование производных изоциановой кислоты при действии кислотных хлорангидридов на гремучую ртуть, также — синтезы альдоксимов из гремучей ртути с фенолами и углеводородами при помощи Al 2Cl6 (Шолль); 5) синтезы фульминатов из монокарбоновых производных, как то: синтез Нефа (из Na-соли нитрометана, "Ann.", 280, 277), Л. Джонса (из основной соли В. Мейера и Риллиэ, HOHgO—HC=NOHg, "Amer. Chem. J.", 20, 27), Байдла (из хлористого ацетилформилоксима и азотнокислого серебра, "Ann. d. Chem.", 310, 19) и Ангелико (из малоновой кислоты, НNO 3 и Hg(NO 3)2, "Atti R. Accad. dei Lincei", Roma [5], 10, 1, 476); 6) Л. Вёлер и Теодорович (1905) выделили впервые безводную гремученатровую соль [В этом виде она оказалась совершенно чистой] и криоскопически нашли частичный вес этой соли в водных растворах отвечающим формуле Нефа-Шолля; к тому же заключению привели авторов и наблюдения молекулярной электропроводности водных растворов гремучекислого натрия. Последние факты — наиболее веские доводы в пользу формулы Нефа-Шолля для Г. кисл.; получение муравьиной кислоты вместо щавелевой при разложении гремучей ртути соляной кислотой, так же как и синтез альдоксимов и изоциановых производных, могут быть допущены и при Штейнеровской формуле, если допустить распад по двойной связи такого непрочного тела как Г. кислота в момент реакции. Формула хлористого формилоксима не доказана, так как нет определения молекулярного веса для этого вещества, разлагающегося уже при 0°; формулы аналогичных: формилсульфатоксима SO 4 H—CH=N—OH и тиоформ гидроксамовой кислоты HS—CH=N—OH — являются проблематичными вследствие отсутствия анализов этих тел. Синтез гремучей ртути из Na-соли нитрометана дает ничтожный выход (5 % теоретического) и потому может рассматриваться как результат побочной реакции; синтезы Джонса и Байдла, при проверке их Л. Вёлером и Теодоровичем, не удались, несмотря на варьирование условий и тщательную проверку. Лей и Кисель (1899) исследовали электропроводность водного раствора гремучей ртути и нашли эту величину чрезвычайно малой:
υ = 513: μ = 0,7(10—7)2.
Авторы думают вследствие этого, что в частице гремучей ртути металл не может быть связан с кислородом, но — либо с азотом, либо — с углеродом, тем более, что величина электропроводности гремучей ртути в водных растворах совершенно подобна такой же величине для цианистой ртути; как гремучая ртуть, так и цианистая, при взбалтывании с амальгамой натрия нацело переходят в гремученатровую соль. Лей и Кисель полагают поэтому, что Г. кислота, подобно другим оксимам, существует в двух таутомерных формах:  и II) Н—С—N=О. Это предположение согласует, по-видимому, противоречивые результаты работ Л. Вёлера и Теодоровича: получение фульминатов из тел определенного лишь строения объясняется тем, что только комбинация двух таутомерных форм одновременно дает стойкую частицу фульмината; величина же частичного веса натриевого фульмината — отвечает мономолекуле. Вероятнее предположить, что таутомерными формами являются: I)
и II) Н—С—N=О. Это предположение согласует, по-видимому, противоречивые результаты работ Л. Вёлера и Теодоровича: получение фульминатов из тел определенного лишь строения объясняется тем, что только комбинация двух таутомерных форм одновременно дает стойкую частицу фульмината; величина же частичного веса натриевого фульмината — отвечает мономолекуле. Вероятнее предположить, что таутомерными формами являются: I) 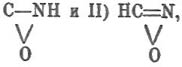 , так как формула H—C—N=O обусловливала бы способность гремучих солей к реакциям прямого присоединения как в том случае, если считать в этой формуле углерод двухатомным,
, так как формула H—C—N=O обусловливала бы способность гремучих солей к реакциям прямого присоединения как в том случае, если считать в этой формуле углерод двухатомным, 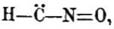 , так и в том случае, если азот принять в ней пятиатомным: H—C ≡ N=O. Как известно, фульминаты мало склонны к реакциям прямого присоединения. Ср. Nef, "Lieb. Annal." (280, 277, 303); Scholl, "Ber." (32, 3492); Stahlschmidt, "Pogg. Ann." (20, 547); Ley и Ki ssel, "Ber." (32, 1364); L. Wö hler и Theodorowitch, "Ber." (38, 1345—1351).
, так и в том случае, если азот принять в ней пятиатомным: H—C ≡ N=O. Как известно, фульминаты мало склонны к реакциям прямого присоединения. Ср. Nef, "Lieb. Annal." (280, 277, 303); Scholl, "Ber." (32, 3492); Stahlschmidt, "Pogg. Ann." (20, 547); Ley и Ki ssel, "Ber." (32, 1364); L. Wö hler и Theodorowitch, "Ber." (38, 1345—1351).
Д. Гр.
| "БРОКГАУЗ И ЕФРОН" >> "Г" >> "ГР" >> "ГРЕ" >> "ГРЕМ" |
Статья про "Гремучая кислота" в словаре Брокгауза и Ефрона была прочитана 1239 раз
| Стейк на сливочном масле |
| Стейк на сливочном масле |
TOP 15
- Волос
- Проно
- Степные животные
- Гимнастика
- Индийский океан
- Архитектура
- Сравнение, в литературе
- Манда
- Клитры
- Колесование
- Испарение
- Травоядные животные
- Оплодотворение у pacтений
- Вредные насекомые
- Электризация тел